「生体の窓」を使った明るい蛍光観察が可能で生体毒性のないバイオマーカーを開発物質・材料研究機構・国際ナノアーキテクトニクス研究拠点 白幡 直人
- 説明文
- 写真
2光子励起では,二つの光子が同時に蛍光体に吸収されることで,2倍のフォトンエネルギーで光励起された場合と同様の現象が生じます。この現象の応用は,特にバイオイメージングの分野で高い関心を集めています。
蛍光法は,肉眼では見ることのできない細胞などを蛍光体で標識して視覚化することで,細胞の分布状態や動態を観察する手法です。中でも「生体の窓」と呼ばれる,光が生体を透過しやすい波長域(650-1000nm)を利用すると,生体の中で起こっている反応を“あるがままの状態(In-vivo)”で観察することが可能となります。生体深部の視覚化は,例えば,神経細胞活動を始めとした脳内で起こる多様な動的現象の理解を深めるなど,基礎研究の発展に大きく貢献しています。このように観察法の技術革新が進む一方で,当該波長域で利用可能な蛍光体の種類は限られます。
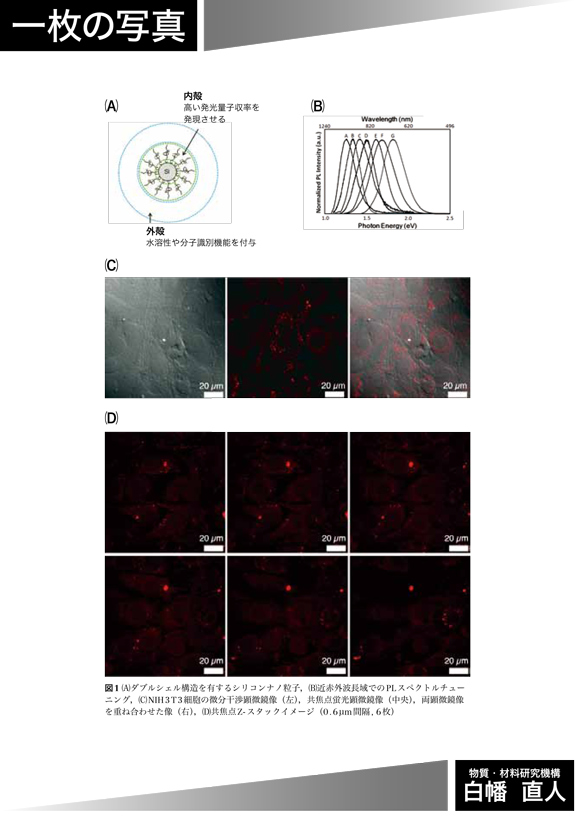
本研究では,シリコン系バイオマーカーを使った「生体の窓」の波長域における2光子励起蛍光イメージングに世界で初めて成功しました1)。シリコンはこれまでにも1光子励起によるバイオイメージング用の蛍光体として利用が検討されてきましたが,発光量子効率が低い等といった問題に悩まされてきました。本研究では,コアである結晶シリコンを炭化水素基と両親媒性分子で覆う,新しいコア・ダブルシェル構造を考案しました(図1A)。コアのサイズを制御することで「生体の窓」波長域で発光波長可変を達成しました(図1B)。
内殻を構成する炭化水素鎖が発光量子収率を増強するメカニズムを解明し,すべての波長帯で発光量子収率30-48%を実現しました。そして,内殻を両親媒性分子で覆うことで水溶性を付与しました。当該バイオマーカーは,蛍光寿命がマイクロ秒と長く自家蛍光の問題を回避できます。シリコンナノ結晶に特徴的な大きな「吸収-発光」ストークスシフトに着眼し,2光子励起したところ「シグナル-背景色」比の高い蛍光イメージング像が得られました。図1Cでは,マウス胎児から分離したNIH3T3細胞が蛍光マーキングされることが確認されました。粒子は細胞基質には取り込まれますが,核には侵入していないことが中央像より分かります。図1Dに示すZ-スタック像から,細胞外および細胞内領域との間の良好なコントラストが見られます。本研究開発のナノ粒子に対する細胞生存率の計測を行ったところ細胞への毒性は,半導体バイオマーカーに比べて,格段に低いことが示されました。
参考文献
1)C. Sourov, et al., Nanoscale 2016, 8, 9009-9019
蛍光法は,肉眼では見ることのできない細胞などを蛍光体で標識して視覚化することで,細胞の分布状態や動態を観察する手法です。中でも「生体の窓」と呼ばれる,光が生体を透過しやすい波長域(650-1000nm)を利用すると,生体の中で起こっている反応を“あるがままの状態(In-vivo)”で観察することが可能となります。生体深部の視覚化は,例えば,神経細胞活動を始めとした脳内で起こる多様な動的現象の理解を深めるなど,基礎研究の発展に大きく貢献しています。このように観察法の技術革新が進む一方で,当該波長域で利用可能な蛍光体の種類は限られます。
本研究では,シリコン系バイオマーカーを使った「生体の窓」の波長域における2光子励起蛍光イメージングに世界で初めて成功しました1)。シリコンはこれまでにも1光子励起によるバイオイメージング用の蛍光体として利用が検討されてきましたが,発光量子効率が低い等といった問題に悩まされてきました。本研究では,コアである結晶シリコンを炭化水素基と両親媒性分子で覆う,新しいコア・ダブルシェル構造を考案しました(図1A)。コアのサイズを制御することで「生体の窓」波長域で発光波長可変を達成しました(図1B)。
内殻を構成する炭化水素鎖が発光量子収率を増強するメカニズムを解明し,すべての波長帯で発光量子収率30-48%を実現しました。そして,内殻を両親媒性分子で覆うことで水溶性を付与しました。当該バイオマーカーは,蛍光寿命がマイクロ秒と長く自家蛍光の問題を回避できます。シリコンナノ結晶に特徴的な大きな「吸収-発光」ストークスシフトに着眼し,2光子励起したところ「シグナル-背景色」比の高い蛍光イメージング像が得られました。図1Cでは,マウス胎児から分離したNIH3T3細胞が蛍光マーキングされることが確認されました。粒子は細胞基質には取り込まれますが,核には侵入していないことが中央像より分かります。図1Dに示すZ-スタック像から,細胞外および細胞内領域との間の良好なコントラストが見られます。本研究開発のナノ粒子に対する細胞生存率の計測を行ったところ細胞への毒性は,半導体バイオマーカーに比べて,格段に低いことが示されました。
参考文献
1)C. Sourov, et al., Nanoscale 2016, 8, 9009-9019




















![研究室探訪vol.30 [奈良先端科学技術大学院大学 サイバネティクス・リアリティ工学研究室]](https://www.adcom-media.co.jp/wp-content/themes/adcom/scripts/timthumb.php?src=/wp-content/uploads/2022/11/laboratory1.jpg&w=80&h=100&zc=1&q=100)